As aminas são substâncias orgânicas constituídas de uma cadeia carbônica ligada a um átomo de nitrogênio. São compostos derivados da amônia (NH3), onde ocorre à substituição de um, dois ou três átomos de hidrogênios por radicais orgânicos (R), que podem ser grupos alquilas ou arilas. Lembrando que grupos arilas são radicais derivados dos alcanos, e arilas derivados de um anel aromático. Dessa forma podemos ter aminas do tipo alifáticas e aromáticas.
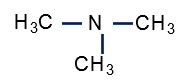
Em função dessa quantidade de hidrogênios que é substituído, podemos classificar as aminas em primarias (R-NH2), secundárias (R1R2NH) e terciárias (R1R2R3N). Nas aminas primárias apenas um dos hidrogênios é substituído por um radical orgânico, como por exemplo, na molécula a seguir CH3 – NH2, nas secundárias temos a substituição de dois átomos de hidrogênios, como no caso de CH3-NH-CH3 e nas terciarias todos são substituídos, conforme exemplificado na estrutura abaixo:
Em relação as suas propriedades, as aminas apresentam caráter básico, sendo substâncias com polaridade intermediárias e as temperaturas de ebulição mais altas que dos alcanos e menores que a dos alcoóis, considerando mesmas massas moleculares. Em relação aos tipos de aminas, as primarias e secundárias podem formar ligações hidrogênio com água ou ainda entre si. Já nas amônias terciárias a formação desse tipo de ligação entre si não é possível, já que todos os hidrogênios foram substituídos por radicais orgânicos e como consequência possuem menores pontos de ebulição quando comparadas com as primarias e secundárias. Em relação à solubilidade em água, as aminas de baixa massa molecular são bastante solúveis em água, e as demais variam de acordo com o tamanho da cadeia.
Nomenclatura das aminas
Para dar nome a amina, de acordo com as regras da IUPAC, existe diferenças entre os tipos de aminas. No caso das aminas primárias podemos seguir o esquema abaixo:
Prefixo + Infixo + Sufixo
O prefixo refere-se à quantidade de carbonos, o infixo ao tipo de ligação, podendo ser an ( ligações simples), en (duplas) ou in (triplas), e o sufixo será a palavra amina. Vamos analisar o exemplo das moléculas abaixo:
CH3-CH2-NH2
Observe que ela tem dois átomos de carbono, então o prefixo fica et, as ligações entre os átomos de carbono são simples, infixo an, e sufixo amina, com isso o nome fica etanamina. Se houver insaturações ou ramificações na cadeia, como é o caso da molécula abaixo, é preciso deixar claro no nome suas posições na cadeia.
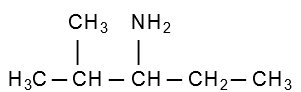
Podemos ver que a cadeia principal contem 5 carbonos, por isso o prefixo será pent, temos uma ramificação no carbono 2 da cadeia, grupo metil, essa cadeia é insaturada, com isso o infixo será an e no carbono 3 está localizado o grupo amina. Com isso teremos o nome 2-metil-pentan-3-amina. Em relação a nomenclatura usual, alguns autores seguem a sequencia:
Nome do radical ou do hidrocarboneto ligado a NH2 + amina
No caso da molécula CH3-CH2-NH2 temos então o nome, etanoamina ou etilamina.
Em relação às aminas secundárias e terciárias, a regra é diferente, pois nesses casos, temos que antes identificar a cadeia mais longa e indicar a posição dos substituintes. Veja o exemplo da molécula de uma amina terciária abaixo:
Nesse caso a numeração e identificação dos radicais ligados ao nitrogênio é representada pela letra N, e a representação dos radicais ligados a cadeia carbônica por números. Primeiro iremos identificar a cadeia mais longa que é uma cadeia com 3 carbonos. A numeração começa da esquerda para direita, e com isso temos um radical metil na posição 2, e um radical metil ligado ao nitrogênio e outro radical etil ligado também ao nitrogênio. Com isso o nome fica, N-etil-2,N-dimetil-propanamina.
As aminas estão presentes em diversas situações de nossa vida, que vão desde a urina, que contem ureia, os aminoácidos que formam nossas proteínas, até os produtos formados pela decomposição, como a putrescina (1,4-diamino-butano) e cadaverina (1,5-diamino-pentano). Algumas aplicações de produtos do grupo amina são utilização em protetor solar, como o ácido p-aminobenzóico (PABA), além de uma série de outros compostos utilizados na produção de medicamento (morfina, fluoxetina), corantes (anilina), substâncias estimulantes, como cafeína, e algumas drogas como cocaína, anfetaminas e nicotina.
Bibliografia:
Tito e Canto. Química na Abordagem do Cotidiano. Volume único, parte C – Química Orgânica. Editora Saraiva 2005.
T. W. Graham Solomons. QUÍMICA. ORGÂNICA volume 1; Sétima edição. Editora LTC livros técnico e científicos, 2000.
T. W. Graham Solomons. QUÍMICA. ORGÂNICA volume 2; Sétima edição. Editora LTC livros técnico e científicos, 2000.
The post Aminas appeared first on InfoEscola.
InfoEscola https://ift.tt/2Sv4GNB
Publicado primeiro em https://www.infoescola.com"
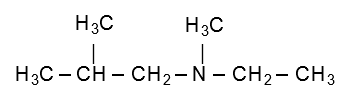
Nenhum comentário:
Postar um comentário